Forskning
Stöd livsviktig njurforskning.
Du kan påskynda nästa forskningsgenombrott
Det behövs ofta massiva forskningsinsatser från många forskare under medverkan av laboratorier och kliniker för att forskningen ska röra sig framåt. Ett större forskningsgenombrott bygger ofta på tusentals smärre forskningsframsteg. Därför går det inte att säga när nästa stora forskningsgenombrott kommer. Det enda vi vet är att det kommer och att du kan påskynda det genom att stödja njurfonden.
Svensk njurforskning nu
Det händer mycket inom svensk njurforskning just nu och det är många forskare som bidrar till framstegen. Extra lovande forskning pågår inom områdena inflammatoriska njursjukdomar och polycystisk njursjukdom. Men det behövs mycket mer pengar om utvecklingen verkligen ska kunna ta fart. 30 miljoner kronor i årligt anslag till njurforskningen har nämnts som en önskvärd nivå av initierade forskare som då är övertygade om att de snabbt skulle nå resultat inom flera områden.
Därför behöver forskarna ditt stöd
- Kronisk njursjukdom (CKD) förekommer hos var tionde svensk och allt fler insjuknar.
- Kronisk njursjukdom leder till bristande kärlfunktion, ofta högt blodtryck och äggvita i urinen, hjärt- kärlsjukdomar som hjärtinfarkt och stroke samt en rad andra följdsjukdomar.
- Trots att kronisk njursjukdom kan betraktas som en folksjukdom med en miljon drabbade svenskar är den inte klassad som en folksjukdom och därför går inte de stora forskningsresurserna till njurforskning.
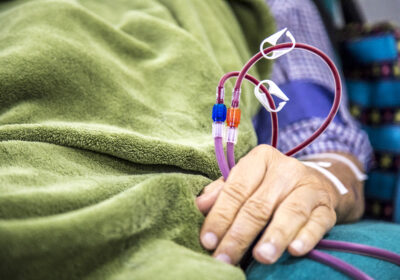
- Dialysbehandling är en mycket resurskrävande livsuppehållande behandling som kan kosta upp mot 1 miljon kronor per år och patient. Stora vinster i minskat lidande och vårdkostnader skulle kunna uppnås om insjuknande i dialyskrävande njursvikt kunde minskas.
Njurfonden stöder
Swisha din gåva
Det går snabbt och enkelt att stötta njurforskningen med Swish. Skanna QR-koden med din mobilkamera eller öppna Swish-appen och ange vårt nummer nedan. Varje gåva – stor som liten – hjälper oss att finansiera viktig forskning och ge hopp till alla som lever med njursjukdom.
900 3674